
【東京】沖縄科学技術大学院大(OIST)のマティアス・ウォルフ准教授と大阪大蛋白質研究所の杉田征彦研究員らの研究グループは17日までに、致死性の高いエボラ出血熱の病原体・エボラウイルスについて、核となる部分の立体構造を原子レベルで解明した。ウイルスを構成するタンパク質同士や、タンパク質とゲノムが結合する仕組みを明らかにし、ウイルス形成を阻害し感染を抑える薬品の開発に発展させられると期待した。論文が18日午前、英科学誌ネイチャーの電子版に掲載される。
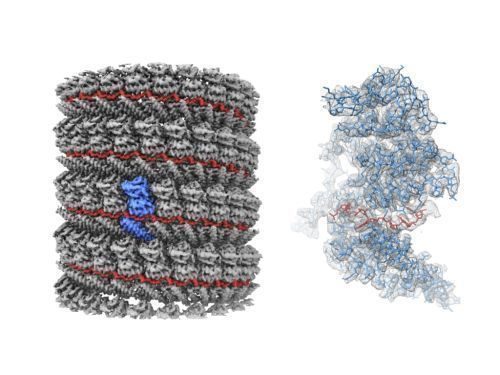
今回の研究はOISTにあるクライオ電子顕微鏡を活用。溶液中の分子を自然に近い状態で観察できる特徴があり、同顕微鏡法の開発に貢献した研究者が昨年ノーベル化学賞を受けた。
研究グループは同顕微鏡を使うことで従来判明していたものの2倍となる解像度でウイルスの核の構造を捉えることに成功した。
従来は不明だった結合の仕組みを明らかにし、結合を阻害する医薬品を開発する際の設計にも役立てられるとする。今回判明した構造は論文公表と同時に国際的なデータベースで公開され、創薬につなげていく。
エボラ出血熱は致死率が最大9割に上るとされ、2013年末から16年にかけて西アフリカで流行し約1万1千人の死者が出た。現在もコンゴ民主共和国で感染が広がっている。予防や治療薬が確立しておらず、対応が課題となっていた。
16日に記者会見した杉田研究員(ウイルス学)は「エボラウイルスは世界の公衆衛生で対策が求められている。治療薬の開発など状況の改善に貢献したい」と研究の狙いを語った。OISTのウォルフ准教授(生物物理学)は「OISTらしい学際的な研究成果が出た。創薬にはできる限り詳細な画像が不可欠で、今回の成果は創薬企業にとって興味深い成果だと思う」と話し、成果の応用に期待した。



